來源 |賽柏藍
世衛組織清單顯示,典型的輻射應急儲備包括以下3種:
穩定碘,用于阻止或減少甲狀腺對放射性碘的吸收;
普魯士藍,用于去除人體內部的放射性銫 (Cs) 和鉈 (Tl);
細胞因子,在急性輻射綜合征(ARS)情況下,用于緩解骨髓損傷的細胞因子;用于治療嘔吐、腹瀉和感染的其他藥物。
下面詳細盤點核輻射治療的8種應急藥品,以及兒童和孕婦的用藥禁忌(第③④⑥種藥品)
第①種,氨磷汀(阿米福汀,WR-2721)是美國Water Reed陸軍醫學研究所經數十年研究推出的輻射防護劑,也是美國食品藥品監督管理局(FDA)許可的第一個輻射防護劑,是目前公認的防護效果很好的藥物, 對較大劑量全身照射有明顯預防效果,能減輕輻射導致的食管炎、肺炎和骨髓抑制。
缺點是有效用藥量較大,毒副反應嚴重。研究還發現,在γ和中子照射前使用氨磷汀可降低癌變和突變的發生。因此,美國國土安全部在核應急醫學準備和響應中建議,初始響應人員在進入放射性爆炸區域前服用氨磷汀,以降低隨機效應的發生。
第②種,雌激素天然甾體激素(如雌二醇)或人工合成的非甾體激素(如己烷雌酚、己烯雌酚等)在臨床和動物實驗中都顯示有一定程度的輻射防護作用,而且輻射前后給藥都有效果。尼爾雌醇是雌三醇的長效制劑,對照射導致的造血系統損傷有明顯的保護作用。
目前,一種稱為5-雄甾烯二醇(5 - AED)的類固醇藥物,引起了人們關注,該藥物化學性質穩定,毒性較低 ,能明顯提高全身輻射小鼠和獼猴的存活率,促進輻射后造血功能恢復以及造血生長因子的表達。美軍放射生物學研究所(AFRRI)已將(5-AED)列入候選輻射防護藥物進行重點研究。
第③種,穩定性碘,可用于預防和阻止放射性碘131對甲狀腺的危害,能阻止和減少甲狀腺對放射性碘的吸收,從而降低甲狀腺的受照劑量。穩定性碘目前主要有2 種,一種為碘化鉀(KI),另一種為碘酸鉀(KIO3),兩者對放射性碘阻吸收的作用基本相同。
為了使甲狀腺受照劑量降到最低,應在攝入放射性碘之前服用穩定性碘,提前6小時服用,幾乎可以提供完全的防護,如果在攝入放射性碘幾小時后,再服用穩定性碘,阻滯效果只有二分之一,且間隔越長,效果越差。穩定性碘的用量與年齡有關,表1(見后文圖片)為WHO推薦的不同年齡組服用穩定性碘的單次劑量。
第④種,二乙烯三胺五乙酸三鈉鋅(Zn-DTPA)和二乙烯三胺五乙酸三鈉鈣(Ca-DTPA),它們能加快釷、 钚及稀土元素等放射性核素從尿中排放,在中毒晚期仍有一定效果,但不能用于放射碘、鈾和镎的促排。
Zn-DTPA和Ca-DTPA不能同時使用,FDA推薦首選Ca-DTPA,如需額外治療,則轉用Zn-DTPA 持續治療。如果是多種方式導致內污染,則靜脈滴注方式效果更好。治療持續的時間可根據內污染程度和患者對治療的反應來確定。在治療過程中應每周檢測污染水平以確定是否終止治療。如果用于孕婦治療,應使用Zn-DTPA
第⑤種,磺酸及巰基絡合劑,主要有2,3-二巰基丙磺酸鈉(Na-DMPS)和二巰基丙醇(BAL)。它們分子中的巰基與金屬離子有較強的結合力,形成無毒性的絡合物從尿中排出,它們可用于210Po、144Pm、14Ce等核素的促排。
用法是:10%BAL油劑,每公斤體重2mg,前二日內4次/d,后3~5天內2次/d,肌肉注射;5%Na-DMPS水劑,每公斤體重5mg,肌肉或皮下注射,2次/d,3~7d為一療程。
第⑥種,普魯士藍,即亞鐵氰化鐵,口服后腸道不吸收,在腸道內選擇性地與攝入的或由腸道腺體再分泌的銫相結合,形成穩定的亞鐵氰化銫鹽,由糞便排出。
美國FDA在2003年批準普魯士藍的用量是:成人和青少年1g/次,3次/d ,連續5d為1療程;兒童(1~12歲)1.0g/d,分2~3次服用。需注意的是有習慣性便秘者和活動性消化道潰瘍或出血者應慎用或禁用。
第⑦種,褐藻酸鈉,它在胃腸道內基本不吸收,可與鍶、鐳和鋇形成穩定的復合物,主要用于這些核素,特別是放射性鍶體內污染。一般制成2%褐藻酸鈉糖漿、3%餅干或6%面包。需在事故后42小時內服用,10g/次。
第⑧種,細胞因子,國內外研究表明,細胞因子如粒細胞-巨噬細胞集落刺激因子(GM-CSF)、粒細胞集落刺激因子(G-CSF)、促紅細胞生長素(EPO)、白細胞介素 I(IL-I)、白細胞介素II(IL-II)、干細胞因子(SCF)等,不僅有放射防護作用,而且能誘導骨髓干細胞增殖、分化,促進造血功能的恢復。
另外,已有動物實驗證明過量碘會造成記憶力下降,因此碘鹽和碘片也需注意用量。


海產品能否食用,需要根據海產品是否來自于受污染海域以及海產品本身的吸收等過程是否受到了放射性污染來判斷。如果海產品中放射性核素的檢測結果符合國際相關標準,說明其對公眾并沒有危害,可以放心食用。
日本福島核事故產生的核廢水主要利用多核素處理系統(advanced liquid processing system,ALPS)進行處理,ALPS可以過濾除3H以外的大部分放射性核素。研究報告表明,經過ALPS處理后的核廢水仍有72%高于日本排放標準(數據截至2019年12月),核廢水中主要含有的放射性核素是3H、少量的1?C、微量的??Sr和13?Cs。
3H(氚)是核電站運行中產生及排放的主要放射性核素之一,其半衰期為12.43年,發生β衰變。
1?C的半衰期為5730年,衰變方式為β衰變——這個放射性核素的影響很小(放射劑量),因為它本身存在于所有碳基物體里,包括人體本身。
13?Cs和13?Cs的半衰期分別為2.06年和30.17年,均能發射β射線和γ射線。
??Sr的半衰期為28.79年,發生β衰變。
有研究結果表明,海洋中魚類、甲殼動物、軟體動物、浮游植物和大型海藻對銫的富集系數分別為 100、50、60、20和50……
如攝入過多放射性核素,也可以通過一些促排藥物將體內攝入的放射性核素排出體外。
如3H被人體攝入后迅速與體內的水達到平衡,導致全身分布,其產生的β射線會對人體造成內照射損傷。可采取服用【茶水和咖啡】等方法減少3H的體內積存量,嚴重者服用【利尿劑(如雙氫克尿噻)】促進3H的排出。
??Sr進入體內后主要沉積于骨骼中,對骨骼和骨髓造成放射性損傷。目前主要采用口服【褐藻酸鈉或氫氧化鋁】的方法來阻止人體對??Sr的吸收。
13?Cs是β射線和γ射線的混合輻射體,極易被人體細胞吸收,且較均勻地分布于全身,特別是軟組織和肌肉組織,主要通過服用【普魯士藍】來阻止放射性銫的體內吸收。
綜合上述信息,福島核廢水的放射性風險主力是3H(氚),這種放射性物質的β衰變會放出高速移動的電子,在皮膚外面不會穿透人體,毒性相對較低,只有大量吸入或者食用,被人體用于細胞代謝,造成內照射,才會嚴重危害健康。
而3H(氚)的生物富集性(大魚吃小魚,人類吃大魚,一層層富集到人體里)遠不如重金屬??Sr和13?Cs兇猛,所以通過喝茶、咖啡或者利尿劑就可以置換排出體外。
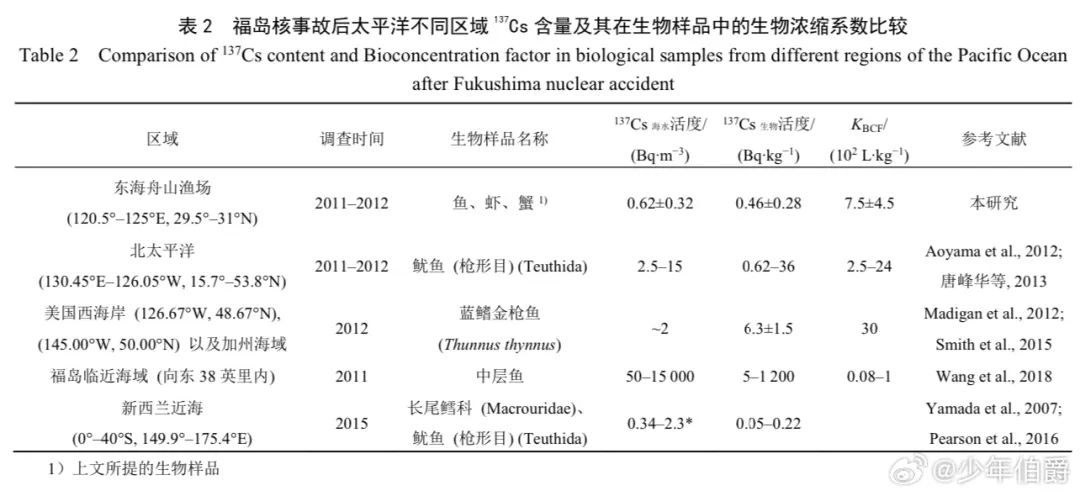
至于微量??Sr和13?Cs的富集問題,就需要看洋流影響了——如5所示,福島海域、北美西海岸和加州海域的放射性重金屬富集(生物濃縮系數)最嚴重,新西蘭近海的影響最小,中國東海受到影響第二小(因為地球最強的洋流黑潮將核廢水往東輸送到了美國西海岸)。